Acerca de la reversión
¿Cómo manejar situaciones que pueden requerir del agente de reversión?
- Revisar la historia clínica donde debemos averiguar: fármaco que toma, grado de adherencia al tratamiento y tiempo desde la última toma.
- Realizar las exploraciones complementarias pertinentes para evaluar el estado de coagulación, comprobar el hemograma y la función renal
- También debe tenerse en cuenta la clasificación del procedimiento a seguir en función de su riesgo hemorrágico.
Clasificación de procedimientos según su riesgo hemorrágico19
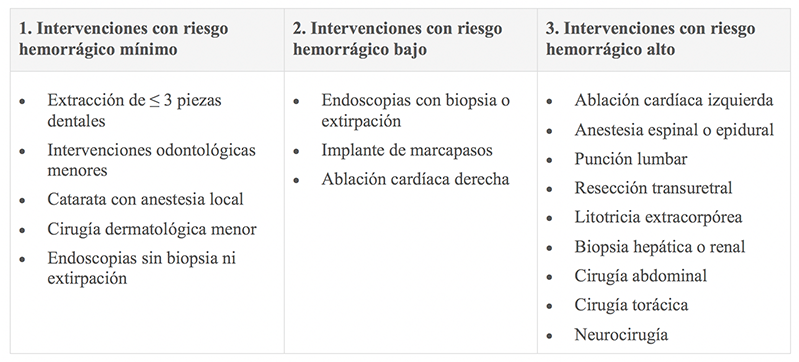
- Además se debe valorar siempre el riesgo hemorrágico e isquémico del paciente. Para esto se proponen 5 categorías basándose en variables clínicas, generando así distintos escenarios y algunas consideraciones generales.
Definiciones de consenso para las categorías de riesgo trombótico perioperatorio24
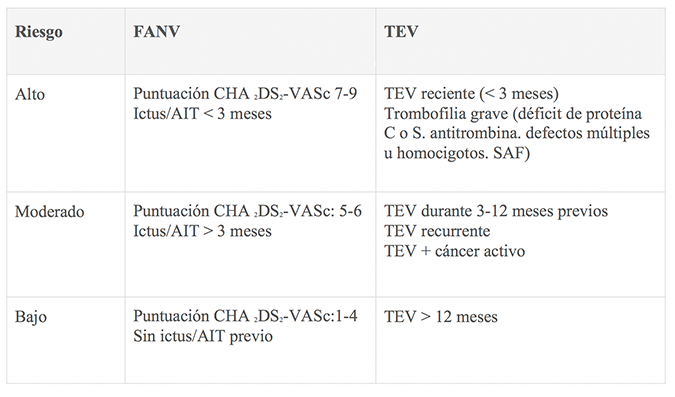
Definiciones de consenso para las categorías de riesgo hemorrágico periprocedimiento24
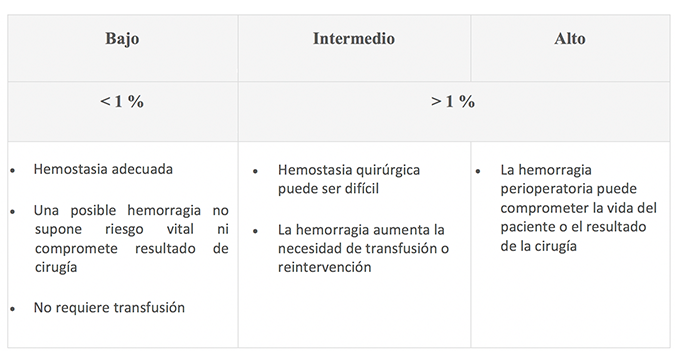
Bibliografía19,24:
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Vivas D, Roldán I, Ferrandis R, Marín F, Roldán V, Tello-Montoliu A, et al. Manejo perioperatorio y periprocedimiento del tratamiento antitrombótico: documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU. Rev Esp Cardiol. 2018;71:553-64.
Niveles plasmáticos y estudios de coagulación en pacientes tratados con ACOD19.
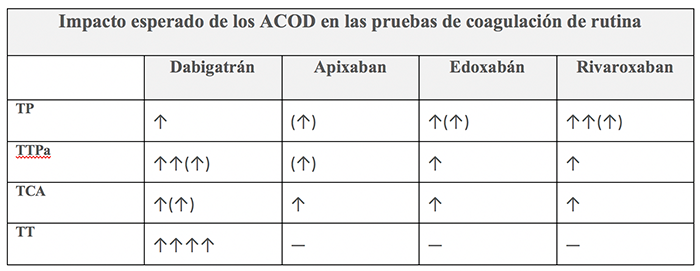
Dabigatrán25:
- Prolonga el TTPa y mínimamente el TT.
- El TTPa solo proporciona una medida cualitativa, pero no cuantitativa.
- El TE proporciona una información más precisa del efecto anticoagulante (más sensible y exacto que el TTPa).
- El TT es muy sensible y útil para detectar la presencia del fármaco en plasma, pero no sirve para monitorizar dosis
- El ensayo del inhibidor de la trombina Hemoclot® puede proporcionar información en Urgencias acerca de la actividad anticoagulante.
Rivaroxaban25:
- Prolonga el TTPa y el TP, y no tiene efecto sobre el TT.
- El INR no es útil para monitorizar los efectos de rivaroxaban.
- La determinación de la actividad antiXa mediante métodos cromogénicos tiene una mayor sensibilidad y precisión que el TP.
Apixaban25:
- Prolonga el TP y el TTPa de manera discreta, con un elevado grado de variabilidad.
- Métodos cromogénicos de medición de actividad antiXa, como el ensayo cromogénico de Rotachrom® Heparin podrían ser útiles en situaciones como sobredosis, hemorragia o cirugía de urgencia.
Edoxabán19:
- Prolonga el TP y el TTPa de manera discreta, con un elevado grado de variabilidad.
- Se puede calcular el efecto en la anticoagulación mediante un ensayo antifactor Xa cuantitativo calibrado que puede ayudar en la toma de decisiones clínicas en situaciones concretas como, por ejemplo, en caso de sobredosis o cirugía de emergencia.
Bibliografía19,25:
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Sánchez M, Escolar G, Reverter JC. Hemorragias en pacientes anticoagulados: utilidad real de los antídotos y modo de actuación con los nuevos anticoagulantes orales. Emergencias. 2013;25:482-90.
En sangrado leve:
- Se pueden controlar retrasando la ingesta del ACOD por un máximo de una dosis.
- En los casos de epistaxis o gingivorragia se puede realizar un tratamiento con agentes fibrinolíticos locales.
- Se debe reconsiderar la elección del ACO y su dosificación.
En sangrado grave que no amenaza la vida:
- Suspensión del anticoagulante oral.
- Las medidas principales a utilizar son el tratamiento de la causa de base y dar medidas de soporte estándar (como compresión mecánica, hemostasia endoscópica o quirúrgica, reemplazo de fluidos, transfusiones y otros).
- Considerar el uso de idarucizumab.
En sangrado grave que amenaza la vida:
- Mismas medidas propuestas en los pacientes con sangrado moderado y además:
- En el caso de dabigatrán considerar el uso de idarucizumab.
- Para los demás ACOD la administración de complejo concentrado protrombínico y complejo concentrado protrombínico activado puede ser una opción (siempre valorando el riesgo tromboembólico) teniendo en cuenta que no cuentan con un agente de reversión comercializado.
Manejo de la Hemorragia asociada al uso de ACOD20
Bibliografía19,20:
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Enriquez A, Baranchuk A, Corbalan R. [Management of bleeding associated with direct oral anticoagulants: update on reversal strategies]. Rev Med Chil. 2019;147:73-82.
Los procedimientos invasivos como la anestesia epidural y la punción lumbar entran en la categoría de "alto riesgo de sangrado" y requieren que el paciente tenga una función hemostática adecuada. Por lo tanto, no se recomienda la realización de este tipo de procedimientos en pacientes bajo tratamiento ininterrumpido con ACOD. De esta manera, se tendrá que interrumpir su administración por hasta cinco vidas medias (correspondiente a 3 días en inhibidores de FXa y de 4 a 5 días para dabigatrán). La anticoagulación podrá reiniciarse 24 horas después de la intervención19. En caso de tener que realizar una punción lumbar sin posibilidad de demora y estar el paciente en tratamiento con dabigatrán, se puede plantear el uso de idarucizumab.
Los pacientes tratados con antitrombóticos para la prevención de complicaciones tromboembólicas a los que hay que realizar una punción lumbar o epidural tienen riesgo de presentar un hematoma epidural o espinal que puede causar parálisis a largo plazo o permanente. El riesgo de estos eventos puede estar aumentado por el uso postoperatorio de catéteres epidurales permanentes o por la administración concomitante de medicamentos que afectan a la hemostasia. Tras retirar el catéter, debe transcurrir un intervalo de al menos 2 horas antes de la administración de la primera dosis de Pradaxa®1.
Se debe controlar con frecuencia la presencia de signos y síntomas de deterioro neurológico (p. ej., adormecimiento o debilidad de extremidades inferiores, disfunción intestinal o vesical). Si se observa afectación neurológica, será necesario un diagnóstico y tratamiento urgente. Antes de la intervención neuroaxial, el médico debe valorar el beneficio potencial frente al riesgo en los pacientes con tratamiento anticoagulante o que van a recibir medicamentos anticoagulantes para la tromboprofilaxis26.
Bibliografía1,19,26:
- Agencia Española de Medicamentos y Productos Sanitarios. Ficha técnica de Pradaxa 150 mg cápsulas duras. 2018. [Consultado en febrero de 2020]. Disponible en: https://cima.aemps.es/cima/dochtml/ft/08442011/FT_08442011.html.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Suero Méndez C. Los nuevos anticoagulantes orales en la fibrilación auricular: preguntas y respuestas para el urgenciólogo. Emergencias. 2013;25:123-36.
Ante la necesidad de una cirugía o un procedimiento invasivo urgente, se recomienda en todos los pacientes realizar una analítica con hemograma, función renal y pruebas de coagulación. Muy importante conocer el tiempo desde que se tomó la última dosis del fármaco.
Para los pacientes tratados con AVK, la intervención o procedimiento se podrá realizar de manera urgente si se obtiene un valor de INR <1,5. Para casos con valores más altos, se tendrá que valorar la urgencia del procedimiento24:
- Si el paciente puede esperar 8–12 horas, bastaría con administrar 10 mg de vitamina K por vía intravenosa.
- En caso de necesidad de cirugía inmediata: se recomienda la administración de concentrado de complejo protrombínico (CPP) 25–50 UI/kg de peso en función del INR actual y objetivo.
Para los pacientes en tratamiento con ACOD, si el estudio de hemostasia muestra actividad anticoagulante, debe plantearse la demora máxima de la cirugía al menos 2 semividas de eliminación del ACOD si la función renal es normal (24 horas), según la situación clínica del paciente. Si se requiere de una intervención inmediata las recomendaciones serían las siguientes24:
- Dabigatrán: Administración de idaricizumab.
- Rivaroxaban, apixaban y edoxabán: CCP 25–50 UI/kg
Como podemos ver, dabigatrán es el único de los ACOD que cuenta con un agente de reversión específico en España. Se trata de idarucizumab (Praxbind®), indicado en caso de requerir intervenciones quirúrgicas de urgencia o procedimientos urgentes o en el caso de hemorragias potencialmente mortales o no controladas13.
El manejo de los pacientes en tratamiento anticoagulante y necesidad de cirugía urgente se recoge en la siguiente figura:
Recomendaciones para el tratamiento de pacientes en terapia anticoagulante que requieren cirugıa urgente24
AVK: antagonista de la vitamina K; ACOD: anticoagulante oral directo; CCP: concentrado de complejo protrombínico; PFC: plasma fresco congelado; SNC: sistema nervioso central; TP: tiempo de protrombina; TTd: tiempo de trombina diluido; TTPa: tiempo de tromboplastina parcial activado; INR: International Normalized Ratio.
Bibliografía24:
- Vivas D, Roldán I, Ferrandis R, Marín F, Roldán V, Tello-Montoliu A, et al. Manejo perioperatorio y periprocedimiento del tratamiento antitrombótico: documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU. Rev Esp Cardiol. 2018;71:553-64.
En consonancia con las recomendaciones para los pacientes en tratamiento anticoagulante oral con warfarina, en aquellos pacientes que estén recibiendo ACOD se necesitará suspender la medicación y hacer un control urgente y adecuado de la tensión arterial para evitar el posible aumento del hematoma. Para los casos de pacientes que se encuentren en tratamiento con dabigatrán y presenten un episodio de HIC, es posible el uso de Idarucizumab como agente de reversión19.
El beneficio o el riesgo de iniciar anticoagulación oral tras una HIC no ha sido investigado en ningún estudio prospectivo, y los pacientes con historial de este tipo de eventos fueron excluidos de los estudios que compararon el tratamiento con ACOD o AVK14.
En pacientes con FA, la anticoagulación oral puede ser reiniciada después de 4–8 semanas, especialmente si se ha tratado la causa o el factor de riesgo de la hemorragia y que dicho tratamiento lleva a menos recurrencias del ictus isquémico y a menor mortalidad. Si se reinicia la anticoagulación, parece razonable considerar un anticoagulante con un riesgo hemorrágico bajo. Adicionalmente, se recomienda valorar la decisión de reiniciar o no el tratamiento con ACO por un equipo multidisciplinario formado por médicos/neurólogos especialistas en ictus, cardiólogos, neurorradiólogos y neurocirujanos teniendo en cuenta las características individuales del paciente14, 19.
Bibliografía14,19:
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur J Cardiothorac Surg. 2016;50:e1-e88.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
En función de la zona y tipo de fractura la clasificación de riesgo hemorrágico será la siguiente27:
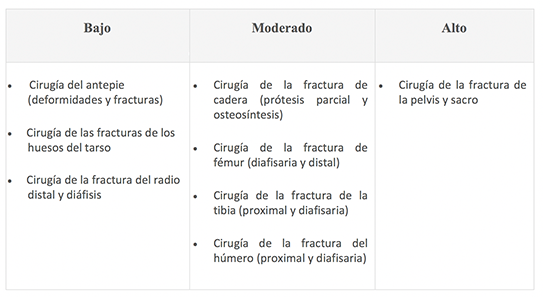
Para el manejo adecuado de dabigatrán en este contexto clínico, debe tenerse en cuenta el riesgo hemorrágico y la función renal del paciente de la siguiente manera24:
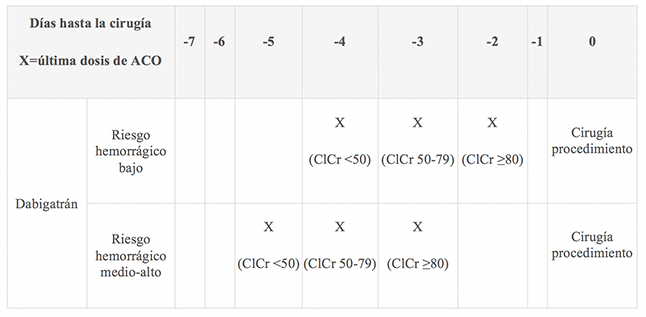
Bibliografía24,27:
- Vivas D, Roldán I, Ferrandis R, Marín F, Roldán V, Tello-Montoliu A, et al. Manejo perioperatorio y periprocedimiento del tratamiento antitrombótico: documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU. Rev Esp Cardiol. 2018;71:553-64.
- SVivas D, Roldán I, Ferrandis R, Marín F, Roldán V, Tello-Montoliu A, et al. Manejo perioperatorio y periprocedimiento del tratamiento antitrombótico: documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU. Material suplementario. Rev Esp Cardiol. 2018;71.
El manejo de la hemorragia digestiva, deberá ir en consonancia con el manejo de cualquier otro tipo de hemorragia en el paciente anticoagulado. Es así como la estrategia de manejo de este tipo de complicaciones en pacientes en tratamiento con ACOD se basa en un análisis de la situación clínica de la siguiente manera19:
- Evaluación del tipo de sangrado: leves, graves que no amenazan la vida, o que amenaza la vida
- Evaluación del paciente y su tratamiento: hora exacta de toma de la última dosis, régimen de dosificación prescrito, función renal, otros factores que influyen en las concentraciones plasmáticas y hemostasia (como la medicación concomitante).
- Evaluación de estado de coagulación mediante pruebas básicas o específicas.
Posteriormente, habrá de realizarse el manejo del episodio hemorrágico según la severidad de la siguiente manera:
Manejo de la Hemorragia asociada al uso de ACOD20
En el caso de un paciente hemodinámicamente estable, que presente hemorragia oculta o hemorragia menor del tracto digestivo inferior, se puede realizar una endoscopia electiva sin interrumpir la administración del ACOD28.
En la mayoría de los casos de hemorragias leves, la anticoagulación se puede reiniciar, simplemente retrasando u omitiendo una única dosis. Todas las otras hemorragias, particularmente aquellas que amenazan la vida, requieren una reevaluación cuidadosa de los riesgos y beneficios de reiniciar anticoagulación19.
En la mayoría de los casos de hemorragias secundarias (p. ej., postraumáticas) o debidas a causas reversibles (p. ej., sangrado genitourinario debido al cáncer) la anticoagulación se puede reanudar una vez que la causa de la hemorragia se haya eliminado19.
En hemorragias graves y que amenazan la vida en las que no se encuentra causa secundaria o reversible clara, los riesgos de reiniciar la anticoagulación puede superar los beneficios19.
Bibliografía19,20,28:
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Enriquez A, Baranchuk A, Corbalan R. [Management of bleeding associated with direct oral anticoagulants: update on reversal strategies]. Rev Med Chil. 2019;147:73-82.
- Chung H, Mutch MG. Special Considerations in the GI Bleeding Patient. Clin Colon Rectal Surg. 2020;33:35-41.
La cardioversión conlleva un riesgo inherente de ictus en pacientes no anticoagulados, lo cual se puede reducir sustancialmente con la administración de tratamiento anticoagulante. Es importante iniciar inmediatamente la anticoagulación de pacientes programados para cardioversión14.
Los pacientes que se han mantenido en FA durante más de 48 h deben comenzar la anticoagulación al menos 3 semanas antes de la cardioversión y después continuar el tratamiento durante 4 semanas (en pacientes hombres con CHA2DS2_VASc de 0 o mujeres de 1) o de manera indefinida (en pacientes hombres con CHA2DS2_VASc ≥ 1 o mujeres ≥ 2). La ACO se debe mantener indefinidamente a los pacientes con riesgo de ictus14, 19.
Cuando se desea realizar una cardioversión precoz, la ecografía transesofágica (ETE) puede excluir la mayoría de los trombos en la aurícula izquierda y permitir la cardioversión inmediata14.
En un subanálisis preespecificado del ensayo RE-LY, se comparó el tratamiento durante al menos tres semanas con dabigatrán (110 o 150 mg cada 12 horas) frente a warfarina en un total de 1.983 cardioversiones (1.270 participantes). En este estudio, no se encontraron diferencias significativas en la tasa de ictus y hemorragia mayor a los 30 días tras la cardioversión (0,8, 0,3 y 0,6%, respectivamente). Por tanto, se concluyó que dabigatrán fue comparable a warfarina en pacientes anticoagulados que requieren cardioversión, siendo la frecuencia de estos eventos baja con ambas dosis de dabigatrán, presentándose como alternativa razonable para los pacientes anticoagulados que requieren cardioversión29.
Bibliografía14,19,29:
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur J Cardiothorac Surg. 2016;50:e1-e88.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Nagarakanti R, Ezekowitz MD, Oldgren J, Yang S, Chernick M, Aikens TH, et al. Dabigatran versus warfarin in patients with atrial fibrillation: an analysis of patients undergoing cardioversion. Circulation. 2011;123:131-6.
La trombolisis intravenosa utilizando el activador del plasminógeno tisular recombinante (rtPA) es el tratamiento de elección en los pacientes que experimentan un ictus isquémico y se ha observado una mayor probabilidad de supervivencia sin discapacidades significativas cuando esta es administrada dentro de las 4,5 horas posteriores al inicio del ictus14, 30.
Para pacientes anticoagulados con AVK la trombolisis solo debe usarse en caso de INR < 1,7. Esta recomendación está basada en el hecho de que el aumento de los valores de INR están asociados a un incremento en el riesgo de hemorragia intracraneal (HIC), aunque no hay evidencia clínica que apoye su uso en rangos específicos de INR14, 30.
En el caso de pacientes en tratamiento anticoagulante con ACOD, y teniendo en cuenta que su vida media oscila entre 8 y 17 h, no se recomienda realizar la trombolisis hasta 24 (o 48) horas después de la última administración del fármaco, tiempo correspondiente a 2–4 vidas medias (esta última es una recomendación de expertos y aún debe ser evaluada en ensayos clínicos). Adicionalmente, los niveles plasmáticos de rivaroxaban, apixaban y edoxabán podrán evaluarse de manera cuantitativa y deberán ser menores a 30ng/mL si son medidos más de 4 horas después de su administración19, 30.
En lo que respecta a la anticoagulación con dabigatrán, el r-TPA también se puede administrar a pacientes tratados con este fármaco si el tiempo de tromboplastina parcial activado (TTPa) es normal y su última toma fue antes de las últimas 48 horas (según consenso de expertos)14. Adicionalmente, existen recomendaciones de expertos que sugieren el uso de idarucizumab como agente de reversión específico de dabigatrán previo a la trombolísis o trombectomía en pacientes con un episodio agudo (< 4,5 horas) de ictus isquémico, cuando la última toma de dabigatránn haya sido < 24 horas (96 h si la TFG<30 ml/mimn)31.
En cuanto al inicio de la anticoagulación después de un episodio de ictus isquémico o un accidente isquémico transitorio (AIT), parece que el riesgo de hemorragia con la anticoagulación parenteral con heparinas excede el beneficio relativo a la prevención del ictus en los primeros días tras uno de estos eventos por lo que estas no deberán ser utilizadas en este contexto14.
El reinicio de la anticoagulación oral después de un episodio ictus isquémico depende de su severidad14, 19.
En aquellos pacientes que han sufrido un ictus grave con riesgo de transformación hemorrágica está aconsejado repetir las pruebas de imagen cerebral para determinar el momento óptimo para iniciar la anticoagulación. De igual forma está recomendado el uso de ACOD sobre los AVK teniendo en cuenta que estos ofrecen mejores resultados en cuanto a la menor incidencia de HIC e ictus hemorrágico14.
Bibliografía14,19,30,31:
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur J Cardiothorac Surg. 2016;50:e1-e88.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Diener HC, Aisenberg J, Ansell J, Atar D, Breithardt G, Eikelboom J, et al. Choosing a particular oral anticoagulant and dose for stroke prevention in individual patients with non-valvular atrial fibrillation: part 2. Eur Heart J. 2017;38:860-8.
- Diener HC, Bernstein R, Butcher K, Campbell B, Cloud G, Davalos A, et al. Thrombolysis and thrombectomy in patients treated with dabigatran with acute ischemic stroke: Expert opinion. Int J Stroke. 2017;12(1):9-12.
La coexistencia de FA con el síndrome coronario agudo (SCA) o la enfermedad coronaria crónica plantea preocupación en el momento de realizar tratamiento conjunto con diferentes fármacos antitrombóticos tras una ICP. Es así como en pacientes que han sido sometidos a este tipo de procedimientos, la doble terapia antitrombótica con ácido acetilsalicílico (AAS) y antagonistas del P2Y12, junto con la adición del tratamiento con anticoagulantes orales para la prevención del ictus en la FA (triple terapia antitrombótica) se asocia con alto y mayor riesgo hemorrágico14, 19.
El estudio RE-DUAL PCI evaluó la seguridad y la eficacia de dos pautas de doble terapia antitrombótica con dabigatrán (150 o 110 mg 2v/d) más un inhibidor del P2Y12 [clopidogrel o ticagrelor] sin AAS frente a la triple terapia antitrombótica con warfarina [más un inhibidor P2Y12 (clopidogrel o ticagrelor) y aspirina (entre 1 – 3 meses)] en 2.725 pacientes con FA tras 120 horas de haber sido sometidos a una ICP. Ambas dosis de dabigatrán (autorizadas para FANV) se evaluaron de manera independiente y la duración de la triple terapia siguió la recomendación de las guías (en función del tipo de stent, el AAS se suspendió 1 mes después de la implantación de un stent metálico convencional y 3 meses después de la implantación de un stent fármaco-activo). La media de días desde la ICP hasta la aleatorización fue de 1,732.
En este estudio, a doble terapia antitrombótica con dabigatrán más un antagonista de P2Y12 redujo de forma significativa el riesgo de hemorragias frente a la triple terapia con warfarina, mostrando no inferioridad en el riesgo de acontecimientos tromboembólicos en general. Las pautas de doble terapia con dabigatrán, usando anticoagulación a dosis completas con dosis de 110 mg o 150 mg dos veces al día, redujeron de forma significativa el riesgo de hemorragias mayores32.
Las recomendaciones más recientes de las sociedades científicas europeas en esta situación clínica son las siguientes33-36:
- Terapia antitrombótica triple (TAT) con AAS, clopidogrel y ACO (De preferencia ACOD) durante 1 mes es la estrategia por defecto en los pacientes en los que se implanta un stent, con independencia del tipo de dispositivo implantado.
- TAT al menos 1 mes en pacientes con alto riesgo isquémico por SCA o con otras características anatómicas o del procedimiento, que supera al riesgo hemorrágico.
- Tratamiento antitrombótico doble (TAD) inicial con ACO (De preferencia ACOD) y clopidogrel (de preferencia) o AAS en pacientes con riesgo hemorrágico elevado y superior al riesgo isquémico.
- En pacientes con FANV debe recomendarse los ACOD de manera rutinaria.
- Los ACOD deben usarse a la mínima dosis efectiva para la prevención del ictus que haya sido evaluada en los ensayos de FA.
- Puede considerarse el uso de la dosis de 15 mg de rivaroxaban (en lugar de 20 mg), aunque su eficacia en la prevención del ictus no ha sido suficientemente evaluada.
- Cuando se usa en TAD, la dosis de dabigatrán preferida es la de 150 mg/12h, a menos estén presentes criterios de reducción de dosis según ficha técnica.
- En caso de usar AVK, el INR objetivo debe estar en el rango bajo y el TRT debe ser > 65%-70%.
- El uso de ticagrelor o de prasugrel como parte del TAT no está recomendado.
- Debería considerarse la interrupción del tratamiento antiagregante y dejar solo ACO (de preferencia ACOD) al cabo de 12 meses tras el procedimiento, aunque puede continuarse añadiendo un antiagregante en casos seleccionados según el riesgo isquémico.
Adicionalmente, en todos los pacientes habría de considerarse y aplicarse dentro de lo posible una serie de medidas que contribuyen a minimizar el riesgo de sangrado y que pueden realizarse antes, durante y después del ICP:
Bibliografía14,19,32-36:
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur J Cardiothorac Surg. 2016;50:e1-e88.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- Cannon CP, Bhatt DL, Oldgren J, Lip GYH, Ellis SG, Kimura T, et al. Dual Antithrombotic Therapy with Dabigatran after PCI in Atrial Fibrillation. N Engl J Med. 2017;377:1513-24.
- Lip GYH, Collet JP, Haude M, Byrne R, Chung EH, Fauchier L, et al. 2018 Joint European consensus document on the management of antithrombotic therapy in atrial fibrillation patients presenting with acute coronary syndrome and/or undergoing percutaneous cardiovascular interventions: a joint consensus document of the European Heart Rhythm Association (EHRA), European Society of Cardiology Working Group on Thrombosis, European Association of Percutaneous Cardiovascular Interventions (EAPCI), and European Association of Acute Cardiac Care (ACCA) endorsed by the Heart Rhythm Society (HRS), Asia-Pacific Heart Rhythm Society (APHRS), Latin America Heart Rhythm Society (LAHRS), and Cardiac Arrhythmia Society of Southern Africa (CASSA). Europace. 2019;21:192-3.
- Angiolillo DJ, Goodman SG, Bhatt DL, Eikelboom JW, Price MJ, Moliterno DJ, et al. Antithrombotic Therapy in Patients With Atrial Fibrillation Treated With Oral Anticoagulation Undergoing Percutaneous Coronary Intervention. Circulation. 2018;138:527-36.
- Knuuti J, Wijns W, Saraste A, Capodanno D, Barbato E, Funck-Brentano C, et al. 2019 ESC Guidelines for the diagnosis and management of chronic coronary syndromes. Eur Heart J. 2019.
- Ruiz-Nodar JM, Luis Ferreiro J. Tratamiento antitrombótico tras revascularización percutánea en pacientes con indicación crónica de anticoagulación oral. REC: interventional cardiology. 2019;1:41-50.
Las hemorragias leves como la epistaxis en pacientes en tratamiento con ACOD no deben subestimarse ya que suelen ser una causa frecuente de interrupción del tratamiento. Los pacientes deben ser informados de los signos y síntomas de una posible hemorragia y se les ha de indicar cuándo consultar en caso de la ocurrencia de un episodio. De igual forma, se les ha de informar el riesgo tromboembólico asociado a una posible interrupción del tratamiento sin indicación médica19.
Al encontrarnos ante un paciente en tratamiento con ACOD y con epistaxis lo primero que debemos hacer es realizar una exploración física del paciente, evaluar los parámetros básicos de coagulación, las posibles interacciones o errores de dosificación y la hora de la última toma del ACOD para la toma de decisiones14.
Las hemorragias leves generalmente se pueden controlar retrasando la toma del fármaco por un máximo de una dosis. En el caso de la epistaxis, puede hacerse un manejo con antifibrinolíticos locales14, 19.
Tratamiento del sangrado activo leve en pacientes que reciben anticoagulación según ESC 2016
Bibliografía14,19:
- Kirchhof P, Benussi S, Kotecha D, Ahlsson A, Atar D, Casadei B, et al. 2016 ESC Guidelines for the management of atrial fibrillation developed in collaboration with EACTS. Eur J Cardiothorac Surg. 2016;50:e1-e88.
- Steffel J, Verhamme P, Potpara TS, Albaladejo P, Antz M, Desteghe L, et al. The 2018 European Heart Rhythm Association Practical Guide on the use of non-vitamin K antagonist oral anticoagulants in patients with atrial fibrillation. Eur Heart J. 2018;39:1330-93.
- ACV: Accidente cerebrovascular
- AIT: Accidente isquémico transitorio
- ClCr: Aclaramiento de creatinina
- AVK: Antagonistas de la vitamina K
- ACOD: Anticoagulantes orales de acción directa
- INR: Cociente internacional normalizado
- CPRE: Colangiografía retrógrada endoscópica
- CCP: Concentrado de complejo protrombínico
- FA: Fibrilación auricular
- FANV: Fibrilación auricular no valvular
- HBPM: Heparina de bajo peso molecular
- SAF: Síndrome antifosfolípido
- SCA: Síndrome coronario agudo
- TCE: Tiempo de coagulación de ecarina
- TP: Tiempo de protrombina
- TT: Tiempo de trombina
- TTd: Tiempo de trombina diluido
- TTPa: Tiempo de tromboplastina parcial activado
- TEP: Tromboembolia pulmonar
- TEV: Tromboembolia venosa
- TPV: Trombosis venosa profunda
DAB1288.12.2019
